- EU ban hành quy định mới liên quan nguyên liệu dùng trong mỹ phẩm
- Thu hồi gần 300 mỹ phẩm chứa chất cấm, có nhiều thương hiệu quen thuộc
- Thu hồi 131 sản phẩm mỹ phẩm của Công ty Vincos Việt Nam sản xuất
Sản phẩm bị thu hồi thuộc nhãn hàng Nivea, do Beiersdorf (Thailand) Co., Ltd sản xuất. Đơn vị chịu trách nhiệm phân phối tại Việt Nam là Công ty TNHH Beiersdorf Việt Nam, trụ sở tại lầu 18, số 72-74 Nguyễn Thị Minh Khai, phường Xuân Hòa, TP. Hồ Chí Minh (trước đây thuộc phường Võ Thị Sáu, quận 3). Lý do thu hồi được xác định là mỹ phẩm lưu thông có công thức không đúng với hồ sơ đã công bố.
 margin: 15px auto;" />
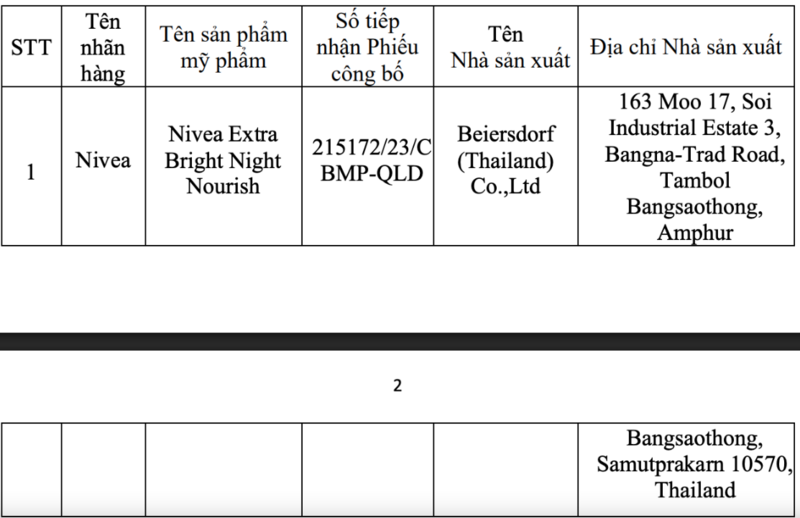
margin: 15px auto;" />Sản phẩm Nivea bị thu hồi trên toàn quốc - Ảnh: Cục Quản lý Dược
Theo hồ sơ do doanh nghiệp gửi ngày 23/12/2025 và 20/01/2026, cơ quan quản lý xác định sản phẩm Nivea Extra Bright Night Nourish (số tiếp nhận Phiếu công bố 215172/23/CBMP-QLD) có chứa Propylparaben với hàm lượng 0,1%. Tuy nhiên, thành phần này không có trong công thức sản phẩm đã đăng ký trong hồ sơ công bố mỹ phẩm trước đó.
Việc này vi phạm quy định quản lý mỹ phẩm, theo đó mọi thay đổi công thức phải được kê khai và phê duyệt trước khi lưu hành.
Cục Quản lý Dược (Bộ Y tế) yêu cầu đình chỉ lưu hành, đồng thời thu hồi toàn bộ sản phẩm Nivea Extra Bright Night Nourishvi trên phạm vi cả nước. Lý do thu hồi được xác định là mỹ phẩm lưu thông có công thức không đúng như hồ sơ đã công bố.
Cục Quản lý Dược đề nghị Sở Y tế các tỉnh, thành phố thông báo đến các cơ sở kinh doanh, sử dụng mỹ phẩm trên địa bàn ngừng ngay việc kinh doanh, sử dụng sản phẩm nói trên và hoàn trả cho đơn vị cung ứng. Đồng thời, các địa phương cần tăng cường kiểm tra, giám sát và xử lý nghiêm các trường hợp vi phạm theo quy định.
Về phía doanh nghiệp, Công ty TNHH Beiersdorf Việt Nam có trách nhiệm gửi thông báo thu hồi đến toàn bộ hệ thống phân phối, tiếp nhận sản phẩm bị trả lại và thực hiện thu hồi, tiêu hủy toàn bộ lô sản phẩm không đáp ứng quy định.
Kết quả thu hồi và tiêu hủy phải được báo cáo về Cục Quản lý Dược trước ngày 20/4. Sở Y tế TP.HCM có trách nhiệm giám sát toàn bộ quá trình này và kiểm tra việc chấp hành pháp luật trong hoạt động kinh doanh mỹ phẩm, báo cáo kết quả trước ngày 5/5.
Ngoài ra, căn cứ Thông tư 06/2011/TT-BYT về quản lý mỹ phẩm, Cục Quản lý Dược cũng quyết định tạm ngừng xem xét và tiếp nhận hồ sơ công bố sản phẩm mới của công ty trong 6 tháng kể từ ngày ban hành văn bản. Sau thời hạn này, nếu doanh nghiệp khắc phục đầy đủ vi phạm, cơ quan quản lý sẽ xem xét tiếp nhận hồ sơ công bố sản phẩm theo quy định.

