Cơ hội và thách thức cho ngành dược khi thực hiện chuẩn EU-GMP
Các nhà máy sản xuất dược phẩm muốn đi vào hoạt động bắt buộc phải đáp ứng các tiêu chí của Bộ hướng dẫn thực hành sản xuất thuốc tốt (GMP – Good Manufacturing Practice) do cơ quan y tế của mỗi quốc gia thẩm định, cấp phép và giám sát (tại Việt Nam là Cục Quản lý dược thuộc Bộ Y Tế).
 margin:0px;" title="Chuẩn EU-GMP mở ra cơ hội tăng trưởng cho ngành dược: Đâu là những cái tên tiên phong?"> margin:0px;" title="Chuẩn EU-GMP mở ra cơ hội tăng trưởng cho ngành dược: Đâu là những cái tên tiên phong?"> |
| Tính đến ngày 11/10/2024, cả nước có 215 nhà máy đạt tiêu chuẩn WHO-GMP, chiếm 89,6% tổng số nhà máy sản xuất dược phẩm |
Hiện trong các tiêu chuẩn GMP phổ biến trong lĩnh vực sản xuất dược phẩm như ASEAN-GMP, WHO-GMP, EU-GMP, Japan-GMP, PIC/S-GMP, US FDA, tiêu chuẩn WHO-GMP là tiêu chuẩn phổ biến nhất tại Việt Nam. Theo thống kê, tính đến ngày 11/10/2024, cả nước có 215 nhà máy đạt tiêu chuẩn WHO-GMP, chiếm 89,6% tổng số nhà máy sản xuất dược phẩm, trong khi ASEAN-GMP – một tiêu chuẩn dễ thực hiện hơn – đã dần trở nên lỗi thời và không còn phổ biến.
Tuy phổ biến, nhưng tiêu chuẩn WHO-GMP hiện không còn được đánh giá cao về độ tin cậy, do các quy định kỹ thuật chưa đủ chi tiết. Ngoài ra, việc thẩm định và chứng nhận WHO-GMP phụ thuộc vào cách áp dụng và hiệu chỉnh của cơ quan y tế từng quốc gia theo trình độ phát triển khác nhau. Vì vậy, cùng một tiêu chuẩn WHO-GMP nhưng các tiêu chí đánh giá và kết quả thẩm định thường không đồng nhất.
Nhiều doanh nghiệp sản xuất dược phẩm Việt Nam hiện đang tập trung cho việc lấy chứng nhận đạt các tiêu chuẩn quốc tế ở mức cao hơn như EU-GMP, Japan-GMP, PIC/S-GMP hoặc US FDA cho các sản phẩm của mình do sự vượt trội mà các tiêu chuẩn này mang lại
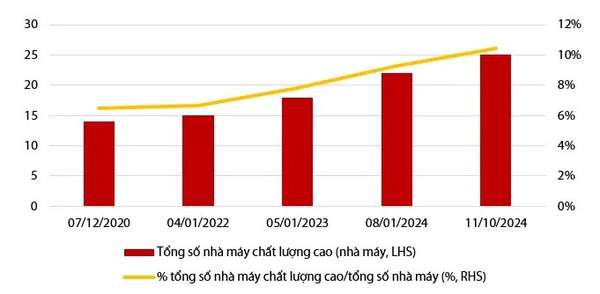 |
| Số lượng nhà máy theo tiêu chuẩn. VDSC Research |
Việc áp dụng tiêu chuẩn EU-GMP mang lại lợi ích lớn cho ngành dược phẩm, giúp sản phẩm được phép lưu hành quốc tế, nâng cao chất lượng và hiệu quả vận hành. Sản phẩm đạt chuẩn này không chỉ tăng định vị thương hiệu mà còn mang lại doanh thu cao hơn, đặc biệt ở kênh OTC và đấu thầu nhóm thuốc chất lượng cao. Theo đó, thuốc được sản xuất theo tiêu chuẩn càng cao sẽ được phân vào nhóm thuốc càng cao, nhờ đó cho doanh thu/lợi nhuận có thể cao hơn 3 lần so với thuốc trúng thầu các nhóm thấp hơn. Thực tế, từ cuối năm 2020 đến tháng 10 năm 2024, cả số lượng nhà máy và tỷ lệ nhà máy đạt tiêu chuẩn cao (EU-GMP, Japan-GMP, PIC-S/GMP) đã tăng đáng kể
Tuy lợi ích của việc “nâng chuẩn” các nhà máy sản xuất dược phẩm trong nước là không nhỏ, một số thách thức làm cho việc thực hiện trở nên không dễ dàng, đòi hỏi nguồn lực và cả mức độ cam kết của các DN. Ước tính chi phí đầu tư cho hệ thống máy móc thiết bị của một nhà máy theo tiêu chuẩn EU-GMP thường cao hơn ít nhất 1,5 - 2 lần so với chi phí đầu tư một nhà máy tương đương theo tiêu chuẩn WHO-GMP, cùng thời gian đạt được chứng nhận kéo dài từ 9 tháng đến 1,5 năm.
Medochemie (Viễn Đông) và Imexpharm (IMP) có lợi thế cạnh tranh nhờ EU-GMP
Tại ngày 11/10/2024, có 25/240 tổng số nhà máy sản xuất dược phẩm tại Việt Nam (chiếm 10,4%) đạt được một trong các chuẩn cao (EU-GMP, PIC/S-GMP, Japan-GMP, US FDA).
Trong số 25 nhà máy thuộc về 16 doanh nghiệp này, Medochemie (Viễn Đông) sở hữu số lượng nhà máy đạt chuẩn cao nhiều nhất. Tuy nhiên, trong số các DN niêm yết trên sàn chứng khoán, Công ty CP Dược phẩm Imexpharm (IMP) hiện có số lượng dây chuyền sản xuất đạt chuẩn cao nhiều nhất với 12 dây chuyền sản xuất tại 3 nhà máy đạt chuẩn EU-GMP
Bên cạnh đó, Imexpharm cũng đang lên kế hoạch triển khai dự án quy mô lớn mang tên "Tổ hợp Nhà máy Dược phẩm Cát Khánh" tại tỉnh Đồng Tháp. Dự án sẽ được phát triển theo tiêu chuẩn EU-GMP trên diện tích 25.000 m2 với tổng mức đầu tư lên tới 1.495 tỷ đồng, trong đó 80% sẽ là vốn vay, tương đương 1.195 tỷ đồng. Khi hoàn thành, nhà máy dự kiến có công suất 1,4 tỷ đơn vị sản phẩm mỗi năm. Thời gian khởi công dự kiến vào quý 3/2025, và nhà máy sẽ bắt đầu hoạt động từ tháng 12/2028 đến quý 1/2030. Đây được coi là một phần quan trọng trong chiến lược nâng cao năng lực sản xuất của Imexpharm, nhằm đáp ứng nhu cầu ngày càng tăng của thị trường dược phẩm trong và ngoài nước.
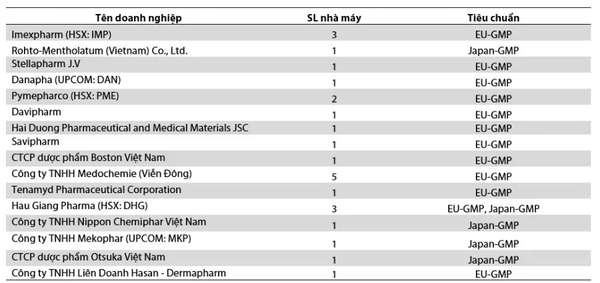 |
| Số lượng nhà máy sản xuất theo tiêu chuẩn cao của các doanh nghiệp (tại ngày 11/10/2024) |
Các doanh nghiệp sở hữu dây chuyền sản xuất đạt chuẩn EU-GMP hoặc các tiêu chuẩn tương đương được đánh giá có tiềm năng tăng trưởng vượt trội, nhờ khả năng sản xuất các loại thuốc có chất lượng cao, đem lại doanh thu và lợi nhuận lớn hơn so với các sản phẩm đạt tiêu chuẩn thấp hơn. Đặc biệt, việc đạt tiêu chuẩn EU-GMP không chỉ giúp doanh nghiệp mở rộng thị trường xuất khẩu mà còn mang lại lợi thế lớn trong đấu thầu tại kênh ETC (kênh đấu thầu thuốc vào các cơ sở y tế công lập).
Theo dự báo của BMI, doanh thu từ kênh ETC dự kiến sẽ tăng từ 76,1% năm 2023 lên 77,4% năm 2028. Sự tăng trưởng này được thúc đẩy bởi chính sách mở rộng độ bao phủ bảo hiểm y tế của Chính phủ, cũng như sự cải thiện về cơ sở vật chất và chất lượng dịch vụ tại các bệnh viện công và tư.
Đặc biệt, các loại thuốc thuộc nhóm đấu thầu cao trong kênh ETC thường mang lại doanh thu và biên lợi nhuận cao hơn, trở thành động lực tăng trưởng mạnh mẽ cho các doanh nghiệp dược phẩm. Trong số các doanh nghiệp niêm yết, Dược phẩm Imexpharm (IMP), Dược Hậu Giang (DHG) và Pymepharco (PME) là những đơn vị nổi bật với lợi thế cạnh tranh nhờ sở hữu các dây chuyền sản xuất đạt chuẩn cao.
Bên cạnh đó, Dược Bình Định (DBD) đang triển khai nhiều dự án nâng cấp dây chuyền sản xuất theo tiêu chuẩn EU-GMP, thể hiện rõ tham vọng đón đầu xu hướng tiêu chuẩn hóa trong ngành dược. Ngoài ra, Dược Hà Tây (DHT) cũng ghi nhận bước tiến quan trọng khi hoàn thành nhà máy mới tại KCN cao Hòa Lạc (Hà Nội) đạt chuẩn Japan-GMP và hiện đang chờ thẩm định.
Nếu các dự án nâng cấp này được hoàn thiện và đưa vào vận hành, đây sẽ là nhân tố thúc đẩy lợi thế cạnh tranh dài hạn, đồng thời mở ra những cơ hội tăng trưởng mới cho các doanh nghiệp trong ngành dược.
 | Thị trường chứng khoán hồi phục, KBSV gọi tên những "ứng viên sáng giá" KBSV dự báo VN-Index có thể chạm vùng 1.305 điểm, khuyến nghị loạt cổ phiếu tiềm năng như VCB, FPT, PNJ, GMD, HPG và REE. ... |
 | EU ép Apple mở cửa Airdrop: Bước ngoặt cho người dùng Android? Liên minh châu Âu muốn Apple mở cửa tính năng AirDrop cho bên thứ ba, cho phép truyền tệp liền mạch giữa iOS và các ... |
Hoàng Anh
Hoàng Anh

